בואו להשפיע עוד היום
"מגזין זמן אמת" הוא אתר תקשורת שהוקם כדי לספק את מה שחסר כל כך במדיה – עיתונות אחרת, מעמיקה, המייצרת תוכן איכותי, שכולל תחקירים, סקירות ומאמרי עומק, ופועלת מתוך תחושת שליחות וללא אינטרסים מסחריים או פוליטיים, בתמיכת הציבור הרחב.
כך הטעה ה-CDC את ועדת המומחים לבטיחות חיסונים: נתוני התמותה על תכשירי ה-RSV לתינוקות הוסתרו וסולפו
בדיון ביוני 2025 על תכשיר ה-RSV החדש של MERCK הציג ה-CDC לוועדה נתונים סלקטיביים ומטעים. תמונת התמותה הכללית מהמחקרים הקליניים – שהצביעה על חוסר איזון עקבי ומשמעותי בשיעורי המוות בין קבוצות הטיפול לקבוצות הביקורת – הוסתרה, אותות בטיחות הושמטו, ומקרי מוות נרשמו בהערות שוליים. התוצאה: הוועדה המליצה ברוב של 2-5 לכלול את התכשיר בחיסוני השגרה לתינוקות


ביוני 2025 התכנסה הוועדה המייעצת החדשה לבטיחות חיסונים בארה"ב (ACIP) לדיון הראשון שלה.
הציפיות הציבוריות מהוועדה, שחבריה מונו על ידי מזכיר הבריאות רוברט פ. קנדי ג'וניור, היו גבוהות: לשקם את תהליך הביקורת של חיסונים חדשים, ולבחון את הראיות לפני ההמלצה על כל חיסון בקפדנות ובאופן שקוף ובלתי תלוי.
אחד התכשירים המרכזיים על סדר היום של הוועדה היה הנוגדן החד-שבטי החדש של חברת Merck למניעת RSV, קלסרובימאב – מוצר הזהה כמעט במבנהו ובפעולתו לנירסבימאב (בייפורטס) של סאנופי ואסטרהזנקה, שאושר לשימוש ב-2023 וכבר נכלל בתוכנית חיסוני השגרה לתינוקות בארה"ב (וממש לאחרונה הוכלל גם בתוכנית חיסוני השגרה לתינוקות בישראל). מוצר שלישי מאותה קבוצה, פליזיבומאב, ניתן כבר מספר שנים אך ורק לפגים ולתינוקות בסיכון.
כעת התבקשה הוועדה להכריע האם להמליץ לכלול גם את התכשיר של Merck, בנוסף על התכשיר של סאנופי/אסטרה זנקה, בתוכנית החיסונים לכלל התינוקות.
אף שרשויות הבריאות מכנות אותם בקמפיינים לציבור הרחב "חיסוני RSV", בפועל, מדובר בנוגדנים חד־שבטיים (monoclonal antibodies) – תרופות ביולוגיות הניתנות בהזרקה. בשונה מחיסונים, תכשירים אלה אינם "מאמנים" את מערכת החיסון להגיב לנגיף, אלא מספקים הגנה פסיבית קצרת טווח, הנמשכת רק עד שרמת הנוגדן בגוף יורדת. הסיבה המרכזית שבגללה הם מכונים "חיסונים" היא בשל העובדה שבארצות הברית, יצרניות החיסונים שנכללים בתוכנית חיסוני השגרה לתינוקות מוגנות על פי חוק מפני תביעות.
לאחר דיון שבמהלכו הציגו נציגי ה-CDC בפני חברי הוועדה נתוני פוסט מרקטינג שהעידו לכאורה על בטיחותו של החיסון, הצביעה הוועדה ברוב של 5-2 בעד ההמלצה. רק שני חברים התנגדו להמלצה – פרופ' רצף לוי וד"ר טרייסי הוג. שאר החברים, כולל יו"ר הוועדה ד"ר רוברט מאלון, השתכנעו שאין חששות בטיחותיים יוצאי דופן.
אך האומנם תחושת הביטחון הזו הייתה מוצדקת, ועל מה בדיוק היא התבססה?
אות הפרכוסים: כיצד הוסתר אות בטיחות מרכזי מהוועדה
במהלך הפגישה הוצגה בפני חברי הוועדה מצגת ובה נתוני בטיחות ממערכת Vaccine Safety Datalink (VSD) של ה-CDC. אחת השקופיות במצגת התמקדה בפרכוסים לאחר מתן נירסבימאב.
הנתונים פוצלו לשתי קבוצות גיל: תינוקות בני 0-37 ימים, ותינוקות בני 38 ימים עד גיל 8 חודשים פחות יום. בכל אחת מהקבוצות נרשם יחס סיכון מוגבר לפרכוסים (3.50 ו-4.38, בהתאמה), אך בשתיהן נקבע כי היחס "לא מובהק", ולכן לא מהווה אות בטיחות.
ואולם, כפי שחשפה לאחרונה ד"ר מריאן דמאסי, ניתוח מאוחד של שתי הקבוצות מוביל לתמונה שונה לחלוטין: עלייה של כמעט פי ארבעה בסיכון לפרכוסים, כשהתוצאה מובהקת סטטיסטית. אלא שניתוח מאוחד זה – ואות הבטיחות החמור שנובע ממנו – לא הוצגו בפני חברי הוועדה.
ההחלטה לקבוע את נקודת החלוקה לשתי הקבוצות דווקא בגיל 38 ימים – בדיוק בנקודה שבה על פי לוחות הזמנים בארה"ב מתחילים חיסוני השגרה לתינוקות – לא הייתה מבוססת על הצדקה ביולוגית ברורה. על ידי פיצול אות הבטיחות לשתי קבוצות קטנות יותר נמחקה למעשה המובהקות הסטטיסטית.
בחירה נוספת ברמת התכנון החמירה את הבעיה עוד יותר. בניתוח ה-CDC נעשה שימוש בשיטת "טווח סיכון עצמאי", שבה רק שבעת הימים הראשונים לאחר ההזרקה סווגו כ"תקופת סיכון". ימים 8-12 הוגדרו כ"תקופת ביקורת". משמעות הדבר היא שכל פרכוס שהתרחש ביום 8 או מאוחר יותר נספר כלא קשור, גם כאשר ייתכן מאוד שלתזמון כזה יש קשר סיבתי סביר למוצר. במעקב תרופתי (פאמרקו ויג'ילנס) מקובל לבחון מספר חלונות זן, ולא רק נקודת חתך צרה אחת.
לשתי הבחירות האלה הייתה השפעה משמעותית. ההצבעה על אישור הקלסרובימאב עברה ברוב של 2-5. אילו היה מוצג בפני חברי הוועדה מידע שלם יותר – דהיינו, הסיכון המאוחד לפרכוסים וחוסר האיזון העקבי באירועים במערכת העצבים ברמת הניסוי – ייתכן שהוא היה מוביל לתוספת של שני קולות, שהיו מספיקים כדי לשנות את ההכרעה לכיוון ההפוך.
החשש, לדברי דמאסי, אינו מוגבל למוצר אחד. בשל הדמיון המבני בין נירסבימאב וקלסרובינאב, הסיכון לפרכוסים משותף כנראה לכל קבוצת התרופות הזו (Class effect). המשמעות היא שההשמטה של האנליזה המאוחדת מנעה מידע מהותי בעל השלכות ישירות על כל נוגדני ה-RSV המצויים כיום בשימוש.
ממצאים אלה נחשפו רק בזכות הניתוח העצמאי של ד"ר דמאסי. ללא עבודתה, ייתכן שהיו נותרים בלתי ידועים – לא רק לציבור, אלא גם לחברי ה-ACIP, שהצביעו בעד הכללת המוצר בתוכנית חיסוני השגרה על סמך המידע החלקי שהוצג להם.
שיעורי התמותה במחקרים לא הוצגו בפני החברים
באופן תמוה, מצגת הבטיחות שה-CDC הציג בפני ועדת ה-ACIP לא כללה התייחסות לסוגיה שאמורה להיות המרכזית ביותר במחקרי הבטיחות הקליניים – נתוני התמותה של שני התכשירים, של סאנופי/אסטרהזנקה ושל מרק. העובדה הזו בולטת במיוחד לאור העובדה שבשני המוצרים נצפה חוסר איזון עקבי ומשמעותי בשיעורי התמותה בין הקבוצות שקיבלו את התכשיר לבין קבוצות הביקורת (שקיבלו פלצבו, או פליביזומאב - הנוגדן שניתן לפגים).
נירסבימאב: תמותה לפי זרוע המחקר
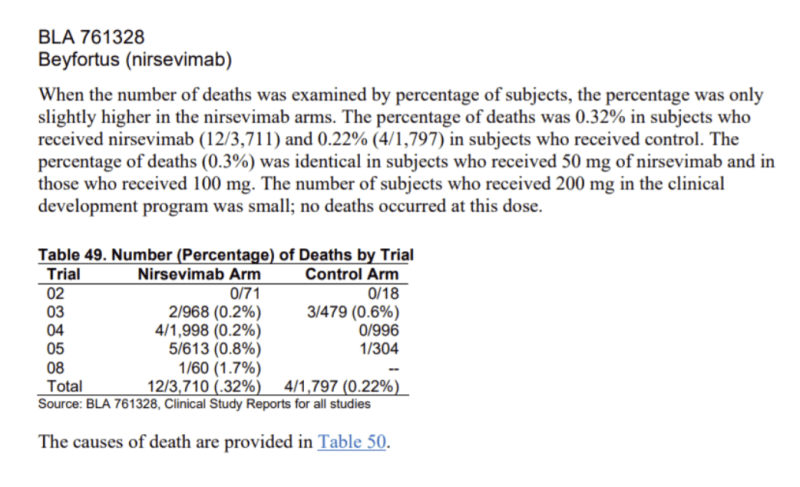
הסקירה המשולבת שערך ה-FDA למחקרים הקליניים בילדים של נירסבימאב, התכשיר של סאנופי ואסטרהזנקה, ציינה במפורש "חוסר איזון בלתי צפוי" במספר מקרי המוות שנצפו בהם. להלן הנתונים (טבלה 49, עמ' 177 בדו"ח):
- מחקר 03 – 2 מקרי מוות מתוך 968 משתתפים שקיבלו נירסבימאב; 3 מתוך 479 בקבוצת הביקורת.
- מחקר 04 (MELODY) – 4 מקרי מוות מתוך 1,998 מקבלי נירסבימאב; 0 מתוך 996 בקבוצת הפלצבו.
- מחקר 05 (MEDLEY) – 5 מקרי מוות מתוך 613 מקבלי נירסבימאב; 1 מתוך 304 שקיבלו פליביזומאב.
- מחקר 08 – מקרה מוות אחד מתוך 60 נירסבימאב; ללא קבוצת ביקורת מקבילה.
בסך הכל דווחו 12 מקרי מוות מתוך 3,710 בקבוצת נירסבימאב לעומת 4 מקרי מוות מתוך 1,797 בקבוצות הביקורת – שיעור תמותה של 0.32% בקבוצות ההתערבות, לעומת 0.22% בקבוצות הביקורת. חוסר האיזון הזה נראה אולי קטן במונחים אבסולוטיים, אבל הוא היה בלתי צפוי – ועקבי באותו כיוון.
קלסרובימאב: תמותה לפי זרוע המחקר
סקירת הסיכונים שערך ה-FDA ב-2025 לגבי קלסרובימיאב, התכשיר של Merck שנדון בוועדת ה-ACIP, מצביעה על מגמה דומה בשני הניסויים המרכזיים שלו:
- מחקר 007 (CLEVER) – 7 מקרי מוות מתוך 2,409 מקבלי קלסרובימאב; 3 מתוך 1,202 מקבלי פלצבו.
- מחקר 008 (SMART) – 8 מקרי מוות בקרב כ-500 מקבלי קלסרובימאב; 4 בקרב כ-500 מקבלי פליביזומאב.
בסך הכל דווחו 15 מקרים בקבוצות שקיבלו קלסרובימאב, לעומת 7 בקבוצות הביקורת (שקיבלו פלצבו או פליביזומאב). למרות שמקרי המוות לא יוחסו למוצר, ה-FDA הכיר במפורש בחוסר האיזון המספרי.
מוות בהערת שוליים
בעדכון על ניסוי MELODY שפורסם בשנת 2023 בכתב העת The New England Journal of Medicine דיווחו החוקרים בגוף הטקסט הראשי של המאמר כי תועדו ארבעה מקרי מוות בזרוע הניסוי שקיבלה את הנירסבימאב, לעומת אפס מקרים בזרוע הפלצבו. הם קבעו שאף אחד מארבעת מקרי המוות אינו קשור לטיפול.
ואולם, עיון מדוקדק בנספח המשלים של הניסוי מגלה תמונה שונה. מתחת לדיאגרמת ה-CONSORT – התרשים התקני שמשקף את שלבי ההשתתפות בניסוי הקליני, החל מגיוס המשתתפים, דרך ההקצאה לקבוצות ועד שלב המעקב – מופיעה הערת שוליים שבה מתועד מקרה מוות חמישי בקבוצת הנירסבימאב. על פי ההערה, ארבעה מקרי מוות שהתרחשו עד היום ה־361 נכללו בניתוח הבטיחות, בעוד שמקרה מוות נוסף, שהתרחש ביום ה־440, הוחרג.
החרגה זו אינה תואמת את פרוטוקול הניסוי עצמו, אשר קבע מראש מעקב בטיחותי של 510 ימים לאחר מתן התרופה. לפי הגדרה זו, מקרה מוות ביום ה־440 נמצא בתוך חלון הבטיחות שנקבע.
במלים אחרות, מקרה מוות חמישי "נקבר" בהערת שוליים בתוך דיאגרמה בנספח למחקר – כך שנדרשה ערנות יוצאת דופן כדי להבחין בו.

עמימות דומה מופיעה גם בניסוי CLEVER של חברת מרק. שבעה מקרי מוות דווחו בזרוע שקיבלה את הקלסרובימאב, ושלושה נוספים בקבוצת הפלצבו – כולם במסגרת תקופת המעקב שנמשכה 365 ימים – אך כולם סווגו כ"לא קשורים" לטיפול.
עם זאת, במצגת של ה-CDC הופיעה גם הערת שוליים המתייחסת למקרה מוות נוסף שהתרחש ביום ה־487, לאחר שהשתתפות התינוק בניסוי הופסקה בהנחיית הרופא. לא ברור האם מקרה זה נכלל במניין שבעת מקרי המוות או הוצג בנפרד.
העובדה שמקרה מוות זה, שהתרחש מחוץ לחלון התצפית, קיבל התייחסות מפורטת, בעוד ששבעת מקרי המוות שהתרחשו בתוך חלון המעקב הוצגו כנתון כולל בלבד – ללא פירוט סיבות המוות או מועדיהם – מצביעה על גישה סלקטיבית לשקיפות. פרקטיקות דיווח מסוג זה מונעות ממבקרים חיצוניים להעריך האם דפוסי התמותה תואמים התפלגות מקרית סבירה, או שמא הם מחייבים בחינה מעמיקה יותר.
אותו דפוס חוזר גם בניסוי SMART של מרק. שם דווחו שמונה מקרי מוות בזרוע שקיבלה קלסרובימאב, לעומת ארבעה בקרב תינוקות שקיבלו פליביזומאב. גם במקרה זה קבעו החוקרים כי אף אחד ממקרי המוות לא היה "קשור" לטיפול, ולא סופק כל פירוט בנוגע למועדיהם או לסיבותיהם.
הסוגיה המרכזית כאן איננה שאלת הסיבתיות, אלא שאלת השקיפות. כאשר מספר מקרי המוות קטן כל כך, חובה שכל אחד מהם יוצג בגלוי במאגר הנתונים הראשי. בפועל, המאמר שפורסם הציג מספר אחד, ואילו בנספח נחשף מספר אחר.
דיווח סלקטיבי כזה שולל מהיועצים ל-CDC את היכולת להעריך כראוי את סיכוני התמותה. בבחינה כוללת של כל הניסויים מתגלה תמונה עקבית ומדאיגה: אף אחד מהם לא תוכנן לזהות הבדלים בתמותה, ומספר המקרים בכל ניסוי קטן. אף על פי כן, בארבעה ניסויים אקראיים נפרדים – בשני מוצרים שונים ובכמה מדינות – נרשם שוב ושוב מספר גבוה יותר של מקרי מוות בזרועות הטיפול בהשוואה לקבוצות הביקורת. העקביות הזו קשה להתעלמות.
כפי שציין פרופ' רצף לוי, אחד משני חברי ועדת ה-ACIP שהצביעו נגד האישור: "ארבעה ניסויים שונים כולם מראים תמותה באותו כיוון".
עבור מוצר שמיועד למתן שגרתי לתינוקות בריאים שנולדו במועד, אפילו אותות בטיחות מתונים אמורים לעורר בדיקה מדוקדקת. במקרה זה, הדבר לא קרה – והתמונה המלאה של מקרי המוות כלל לא הוצגה בפני הוועדה.
כאשר מספר מקרי המוות כה קטן, הציפייה הבסיסית היא לפירוט מלא ושקיפות מוחלטת – אך אלה לא התקיימו.
סיבות המוות שלא נחשפו
תדרוך מלא ושקוף לוועדת ה-ACIP היה צריך לכלול לא רק את מניין מקרי המוות בכל זרוע ניסוי, אלא גם טבלה מסודרת המפרטת את סיבת המוות, המועד והשיוך לזרוע הניסוי עבור כל מקרה בנפרד. רמת פירוט כזו נחשבת חיונית לפי הסטנדרטים המתודולוגיים והרגולטוריים הנהוגים כיום. העדכון לשנת 2022 בהנחיות CONSORT Harms, שהן הרחבה לרשימת הכללים התקנית של CONSORT לדיווח על ניסויים קליניים מדגישה את הצורך בדיווח מלא ומוגדר מראש של נזקים בניסויים קליניים אקראיים. באופן דומה, הנחיית ICH E9(R1) מדגישה את החשיבות שבהגדרת estimands (במילים פשוטות: התוצאה המדויקת שהניסוי טוען למדוד) ובביצוע ניתוחים שקופים המאפשרים בדיקה עצמאית – במקום להסתפק בהערכות נרטיביות.
אף על פי כן, הסיכומים הפומביים של ה-FDA מתבססים בעיקר על אמירות נרטיביות שלפיהן מקרי המוות "לא קשורים" לטיפול, מבלי להציג פירוק לפי זרועות הניסוי שהיה מאפשר למבקרים חיצוניים לבדוק התכנסויות חריגות לפי מועד, תסמונת או מחלות רקע. הן ה-CDC והן יצרני המוצר לא סיפקו לוועדה טבלה השוואתית כזו.
פער זה איננו תאורטי. כך למשל, במחקר 03 של נירסבימאב (ניסוי שלב 2b) יוחסו שני מקרי המוות בזרוע שקיבלה את התרופה לגסטרואנטריטיס בתינוקות בריאים לכאורה – האחד ביום 143 והשני ביום 338. תמותה מגסטרואנטריטיס בתינוקות בריאים היא תופעה חריגה ביותר בעידן הרפואה המודרנית, ולכן הופעתה בשני מקרים בתוך אותה זרוע ניסוי מעוררת סימני שאלה. בהיעדר טבלה שקופה לפי זרועות ניסוי, שבה מפורטים סיבות המוות והמועדים, יחד עם בדיקה סטטיסטית בסיסית של חוסר האיזון הכולל, היועצים אינם יכולים לקבוע אם מדובר בסטייה אקראית או באות בטיחות משמעותי המחייב חקירה נוספת.
מקור נתונים יחיד: ה-CDC הציג נתוני בטיחות ממקור אחד בלבד
בדיון ה-ACIP ביוני 2025, ה-CDC הציג לחברי הוועדה סקירת בטיחות שהתבססה אך ורק על נתוני ה־Vaccine Safety Datalink (VSD) – מערכת מעקב פעילה שמאגדת רשומות רפואיות מ־13 מערכות בריאות בארצות הברית. לא הוצגו כלל נתונים מ־VAERS או מ־MedWatch של ה־FDA, אף שההנחיות הפדרליות קובעות במפורש חלוקה ברורה: כאשר נוגדן ל־RSV ניתן לבדו, תופעות הלוואי אמורות להירשם ב־MedWatch; כאשר הוא ניתן יחד עם חיסונים אחרים, הדיווח אמור להיכנס ל־VAERS.
המשמעות היא ש-CDC הציג לוועדה תמונת בטיחות ממערכת אחת בלבד. זווית ראייה צרה כזו עלולה להחמיץ אותות שמופיעים לראשונה במערכת ניטור אחרת – וזו בדיוק הסיבה לכך שהצלבה בין מקורות שונים נחשבת לדרישת יסוד בפרמקו־ויג'ילנס (ניטור תרופתי).
הסלקטיביות הזו לא נעצרה בארצות הברית. נתוני עולם־אמיתי עצמאיים מצרפת, שהוצגו על ידי החוקרת הלן בנון, ממחישים את החשיבות של נקודת מבט רחבה. במהלך ההשקה הארצית הראשונה של נירסבימאב בסתיו 2023, נרשם דפוס תמותה בולט בתינוקות בני 2-6 ימים:
בספטמבר ואוקטובר 2023, עם תחילת ההפצה הארצית, נרשמו עליות חדות במספר מקרי המוות: 55 ו־62 בהתאמה. בנובמבר, כאשר האספקה צומצמה והחלוקה הוגבלה, ירד המספר ל־26. אולם עם חידוש ההפצה בדצמבר ובינואר, נרשמה שוב עלייה חדה: 50 ו־52 מקרי מוות – שניהם שיאים מובהקים סטטיסטית.
השינויים הללו תאמו מקרוב את דפוסי ההפצה והמגבלות באספקה – ומעידים על התכנסות זמנית (temporal clustering) שאמנם איננה מוכיחה סיבתיות, אך מהווה אות משמעותי. דפוסים כאלה מהעולם האמיתי – יחד עם ההסתייגויות לגבי מגבלות שיטת המחקר – היו צריכים להיות מוצגים לצד נתוני ה-VSD האמריקאיים, אך הושמטו מתדרוך ה-ACIP.
במבט כולל, החסרת האותות – הן אלו המקומיים והן הבין־לאומיים – הובילה לכך שחברי הוועדה נחשפו רק לגירסה מצומצמת ומרגיעה של המידע הזמין, ולא לתמונה המלאה.
נקודת עיוורון מובנית: הכפילות בסיווג יצרה פרצה במערכת הדיווח
מעבר למה שהוצג ל-ACIP, מסתתרת בעיה מהותית יותר – עצם הסיווג של נוגדנים חד-שבטיים ל-RSV. מבחינה פרמקולוגית אלה תרופות ביולוגיות, ואכן, לצורכי חיוב ותשלום הן מוגדרות כתרופות, אך לצורכי אחריות משפטית הן שובצו בלוח החיסונים לילדים, מה שמעניק ליצרנים חסינות מתביעות במסגרת National Vaccine Injury Compensation Program. לצורך דיווח בטיחות נעשתה חלוקה: כאשר הן ניתנות לבדן, ההנחיה היא להפנות את הדיווח למערכת ה-MedWatch. כאשר הן ניתנות יחד עם חיסונים אחרים, הדיווח מועבר ל-VAERS.
זהות כפולה זו יוצרת מה שמומחים מכנים "נקודת עיוורון בדיווח". בפועל, צוותים רפואיים נוטים לדווח ל־VAERS כאשר מדובר בתינוקות. אלא שפרמקולוגית לא מדובר בחיסון, ולכן במערכת VAERS אין שדה ייעודי לנירסבימאב או לקלסרובימאב. כתוצאה מכך, דיווחים עלולים להירשם בקטגוריה כללית של "סוג חיסון לא ידוע", או להישאר רשומים אך ורק במסד הנתונים של ה-FDA לתרופות, מבלי להגיע כלל ליחידת בטיחות החיסונים של ה-CDC. במצב כזה, אירועים עלולים פשוט להיעלם מן המערכת – ובכך להחמיץ את אותות האזהרה הראשוניים שאמורים להתריע על בעיות בטיחות.
כתוצאה מכך, אירועים עלולים ליפול בין הכיסאות או שלא להיתפס כלל – ובכך לסכל את מטרת המערכת, שנועדה לאתר אותות אזהרה מוקדמים.
מעבר לנתונים: הסתרות ומניפולציות ערערו את האמון ב-ACIP
המידע שהוסתר ביוני 2025 לא היה הערות שוליים טכניות, אלא החלטות שעיצבו את האופן שבו הוצגו הראיות בפני מי שאמונים על שמירת בריאות הציבור. חברי ועדת ה-ACIP קיבלו ניתוחים חלקיים שמסגרו את הסיכונים כמינוריים, בעוד שמידע רחב ומדאיג יותר כלל לא הונח על שולחנם.
אם הוועדה המייעצת, שגובשה תוך התחייבות לעצמאות, יכולה עדיין להיות מושפעת מהצגת מידע מטעה ומגמתית – הבעיה רחבה הרבה יותר מנוגדן יחיד, או מתכשיר כזה או אחר. השאלה האמיתית היא האם ה-ACIP מסוגל למלא את תפקידו כגוף עצמאי באמת, השוקל סיכונים ותועלות, והאם הציבור יכול לבטוח בכך שיגן על התינוקות בשקיפות מלאה.
בואו להשפיע עוד היום
"מגזין זמן אמת" הוא אתר תקשורת שהוקם כדי לספק את מה שחסר כל כך במדיה – עיתונות אחרת, מעמיקה, המייצרת תוכן איכותי, שכולל תחקירים, סקירות ומאמרי עומק, ופועלת מתוך תחושת שליחות וללא אינטרסים מסחריים או פוליטיים, בתמיכת הציבור הרחב.
תגובות לכתבה זו יועברו לאישור לפני פרסום. אנא השתמשו בשפה מכבדת ואם מצאתם טעות, אנא צרפו נימוק ענייני וקישור למקור הטענה.

Report

בצעד חריג: שופט פדרלי בארה"ב ביטל את החלטות ועדת החיסונים ועצר את פעילותה
הצו חוסם את הרפורמה במדיניות החיסונים שהוועדה החלה לקדם, וניתן יומיים לפני דיון על מגבלות הניטור והערכת הבטיחות – דיון עם השלכות על שוק של מיליארדים

ה-CDC מצמצם דרמטית את תוכנית החיסונים בארה"ב, בעקבות צו נשיאותי של טראמפ
השינויים מגיעים גם על רקע בחינה של הפרקטיקות ותוכניות החיסונים הנהוגות במדינות אחרות, והתייעצות עם מומחים בדנמרק, גרמניה ויפן. לעומת זאת, על פי גורמים בממשל, לא הייתה התייעצות עם נציגי חברות התרופות

מהפך בעמדת ה-CDC: הסוכנות מודה – הטענה "החיסונים אינם גורמים לאוטיזם" לא התבססה על ראיות
לראשונה מזה שני עשורים, ה-CDC מודה כי המחקרים הקיימים אינם שוללים קשר אפשרי בין חיסוני תינוקות לאוטיזם, וכי שאלות מרכזיות ביחס לחיסוני תינוקות מעולם לא נבדקו כראוי. המהלך מסמן שינוי משמעותי בשיח של רשויות הבריאות על בטיחות חיסונים, מערער על הנרטיב של "המדע מיושב" ששולט בעשורים האחרונים, ומדגיש את המורכבות האמיתית של אי ודאות מדעית
סערה בארה"ב: ה-FDA צפוי להציג סקירה על 25 מקרי מוות בילדים לאחר חיסוני הקורונה
גורמים מתוך ה-FDA הדליפו פרטים על סקירה מעמיקה המקשרת 25 מקרי מוות בילדים לחיסוני קורונה – לקראת דיון מפתח בוועדה המייעצת של ה-CDC בשבוע הבא. במקביל, רשמו מניות פייזר ומודרנה ירידות חדות

ה-CDC מעודד גברים טרנסג'נדרים "להניק" – אך מתעלם מסיכונים בריאותיים חמורים לתינוקות
ה-CDC זוכה לביקורת קשה לאחר שהתברר שהסוכנות מעודדת גברים טרנסג'נדרים "להניק" – מבלי להזכיר סיכונים בריאותיים חמורים אפשריים לתינוקות. זאת, למרות היעדר מחקרים על בטיחות הפרקטיקה ותופעות לוואי לטווח ארוך, ואף שהתרופה שבמרכז הטיפול להשראת הנקה אינה מאושרת בארה"ב וה-FDA ורשויות נוספות מזהירים משימוש בה בשל סיכון קרדיאלי

ה-CDC מדווח על 8 מקרי מיוקרדיטיס בילדים בני 5-11 לאחר חיסון פייזר. 58 דיווחים על תופעות לוואי בגילאים אלה סווגו כחמורות
מספר הדיווחים בקרב הילדים הצעירים בגילאי 5-11 עלתה פי 2 בתוך חודש וחצי, מאז תחילת מסע החיסונים בקבוצת גיל זו. 58 מקרים סווגו כחמורים - עלייה של 40% מלפני 3 שבועות. בין הדיווחים, ילד בן 7 לקה באירוע לב חמור שלוש שעות לאחר שקיבל את חיסון פייזר, ועל פי הדיווח למערכת ה-VAERS מטופל באקמו
בואו להשפיע עוד היום
"מגזין זמן אמת" הוא אתר תקשורת שהוקם כדי לספק את מה שחסר כל כך במדיה – עיתונות אחרת, מעמיקה, המייצרת תוכן איכותי, שכולל תחקירים, סקירות ומאמרי עומק, ופועלת מתוך תחושת שליחות וללא אינטרסים מסחריים או פוליטיים, בתמיכת הציבור הרחב.